Résumé rapide : L'analyse prédictive dans les essais cliniques utilise la modélisation statistique, l'apprentissage automatique et les données historiques pour prévoir les résultats des patients, optimiser la conception des essais et améliorer l'efficacité du recrutement. Les recommandations de la FDA soutiennent désormais les modèles prédictifs basés sur l'IA pour la prise de décision réglementaire, avec des cadres de validation garantissant la précision des modèles grâce à des indicateurs tels que la pente de calibration et les scores de Brier. Les organisations qui mettent en œuvre ces outils constatent des délais plus courts, une meilleure stratification des patients et une réduction des coûts de développement.
Les essais cliniques ont longtemps constitué la phase la plus coûteuse et la plus longue du développement d'un médicament. Les approches traditionnelles reposent largement sur des analyses rétrospectives et des estimations, même approximatives, des réponses des patients, de la faisabilité du protocole et des délais de recrutement.
Mais cela change rapidement.
L'analyse prédictive applique désormais des techniques statistiques et des algorithmes d'apprentissage automatique aux données d'essais cliniques actuels et historiques, permettant ainsi aux chercheurs d'anticiper les résultats. La FDA a pris acte de cette évolution et a publié des recommandations officielles sur l'utilisation de l'intelligence artificielle tout au long du processus de développement des médicaments et de la conception des essais cliniques.
L'industrie pharmaceutique se tourne de plus en plus vers ces approches basées sur les données pour tout, de l'identification de nouvelles cibles thérapeutiques à la prévision des délais des essais cliniques. En clair : les organisations qui maîtrisent l'analyse prédictive constatent des améliorations mesurables en termes de taux de réussite des essais, de rapidité de recrutement et d'efficacité globale.
Ce que l'analyse prédictive signifie réellement pour les essais cliniques
L'analyse prédictive applique des techniques statistiques et de modélisation aux données actuelles et historiques, permettant ainsi d'anticiper les événements futurs avec des niveaux de confiance quantifiables. Dans le contexte des essais cliniques, cela se traduit par la prévision des taux d'inclusion des patients, l'estimation des risques d'abandon, l'identification des patients susceptibles de répondre au traitement et l'évaluation de la faisabilité du protocole avant d'engager des millions dans sa mise en œuvre.
Selon les recommandations de la FDA, l'intelligence artificielle désigne les systèmes informatisés capables de formuler des prédictions, des recommandations ou des décisions influençant des environnements réels ou virtuels. Ces systèmes perçoivent les environnements grâce à diverses données d'entrée, transforment ces perceptions en modèles par le biais d'analyses automatisées et utilisent l'inférence de ces modèles pour proposer des options concrètes.
La pile technologique est désormais dominée par les Large Medical Models (LMM) et les Multi-modal Foundation Models intégrés à l'apprentissage automatique traditionnel pour la génération de preuves cliniques.
Les composants qui permettent son fonctionnement
Les modèles de prédiction clinique suivent un processus de développement structuré. Les recherches publiées dans les revues médicales décrivent sept étapes critiques : la détermination du problème de prédiction et la définition des prédicteurs et des résultats, le codage approprié des prédicteurs, la spécification de l’architecture du modèle, l’estimation des paramètres du modèle, l’évaluation des performances du modèle, la validation à l’aide d’ensembles de données externes et la présentation du modèle dans un format cliniquement utile.
Les cadres de validation actuels de 2026, y compris la déclaration TRIPOD+AI mise à jour, privilégient l'ordonnée à l'origine/la pente de l'étalonnage et l'analyse de la courbe de décision (DCA) par rapport aux différences R² rigides, nécessitant des facteurs de réduction adaptés à l'impact clinique spécifique.

Utilisez l'analyse prédictive dans les essais cliniques grâce à l'IA supérieure
IA supérieure elle exploite des données structurées et non structurées pour construire des modèles prédictifs qui soutiennent la planification, le suivi et l'analyse des essais cliniques.
L'accent est mis sur les modèles qui s'intègrent aux flux de travail réglementés et qui peuvent gérer des ensembles de données complexes utilisés dans les environnements cliniques.
Vous souhaitez appliquer l'analyse prédictive aux essais cliniques ?
AI Superior peut vous aider avec :
- évaluation des données cliniques et de recherche
- construction de modèles prédictifs
- intégrer les modèles aux systèmes existants
- affiner les résultats en fonction de l'utilisation
👉 Contactez l'IA supérieure pour discuter de votre projet, de vos données et de votre approche de mise en œuvre
Là où l'analyse prédictive a le plus grand impact
Ces applications couvrent l'intégralité du cycle de vie des essais cliniques. C'est là que les organisations constatent les retours sur investissement les plus significatifs.
Recrutement des patients et sélection des sites
Trouver les patients adéquats demeure l'un des principaux obstacles à la recherche clinique. Les modèles prédictifs analysent les dossiers médicaux électroniques, les données de remboursement et les informations des registres afin d'identifier les populations candidates répondant aux critères d'inclusion. Plus important encore, ces modèles prévoient quels centres recruteront le plus rapidement en fonction de leurs performances passées, des caractéristiques démographiques des patients et de la prévalence locale de la maladie.
La différence entre une stratégie de recrutement bien ciblée et une stratégie mal planifiée peut se traduire par des mois de décalage dans les délais et des centaines de milliers d'euros gaspillés en frais de sélection.
Optimisation du protocole et évaluation de sa faisabilité
Avant de finaliser un protocole, l'analyse prédictive permet de simuler des milliers de scénarios d'essai, en testant différents critères d'inclusion, calendriers de visites, sélections de critères d'évaluation et exigences en matière de taille d'échantillon. Cette approche informatique identifie les défauts de conception qui, autrement, n'apparaîtraient que des mois après le début de l'étude.
Les recherches sur les modèles pronostiques de la sclérose en plaques ont montré que de nombreux modèles publiés incluent des prédicteurs rarement mesurés en soins primaires, ce qui limite considérablement leur utilité pratique. L'évaluation de la faisabilité prédictive permet de détecter rapidement ces lacunes de mise en œuvre.
Prise de décision intérimaire et conceptions adaptatives
Les analyses de validation fondées sur des essais cliniques achevés et des données réelles permettent désormais de sélectionner des modèles prédictifs et des règles d'analyse intermédiaire pour les études futures. La FDA a pris acte de cette demande, soulignant que l'IA et l'apprentissage automatique gagnent du terrain dans la recherche clinique et transforment le paysage des essais.
Les essais adaptatifs utilisent l'accumulation de données pour modifier des aspects tels que la taille de l'échantillon, les groupes de traitement ou les populations de patients en cours d'étude. L'analyse prédictive sous-tend ces décisions, garantissant que les modifications améliorent l'efficacité sans compromettre la rigueur statistique.
Surveillance de la sécurité et prédiction des événements indésirables
Les modèles d'apprentissage automatique entraînés sur des bases de données historiques de sécurité peuvent identifier les patients présentant un risque élevé d'événements indésirables spécifiques avant même leur survenue. Ceci permet la mise en place de protocoles de surveillance proactive, des échanges plus éclairés sur le consentement éclairé et une intervention plus précoce dès l'apparition des signes avant-coureurs.
L'étalonnage de ces modèles de sécurité est primordial. Des prédictions mal étalonnées entraînent soit une saturation d'alarmes due à des faux positifs, soit des signaux manqués dus à des faux négatifs.
Normes de validation et considérations réglementaires
Les lignes directrices de la FDA de 2024 relatives à l'utilisation de l'intelligence artificielle pour faciliter la prise de décision réglementaire concernant les médicaments et les produits biologiques définissent des exigences claires. Les promoteurs doivent démontrer que les modèles prédictifs sont adaptés à l'usage prévu, correctement validés et documentés de manière transparente.
La performance d'un modèle ne se résume pas à sa précision. L'étalonnage est primordial en contexte clinique. Les prédictions d'un modèle bien étalonné correspondent aux résultats observés sur l'ensemble du spectre de probabilité. À l'inverse, les modèles mal étalonnés peuvent présenter une forte discrimination (capacité à distinguer les événements des non-événements) tout en surestimant ou sous-estimant systématiquement le risque absolu.
L'évaluation de l'étalonnage consiste généralement à ajuster une droite d'étalonnage aux observations par rapport aux prédictions, résumant la performance par deux nombres : l'ordonnée à l'origine et la pente. Il existe également des courbes d'étalonnage lissées qui permettent d'évaluer l'étalonnage local selon différentes strates de risque.
Exigences de validation externe
La validation interne sur l'ensemble de données de développement ne suffit pas. Les modèles de prédiction doivent démontrer leur applicabilité à de nouvelles populations, à différents contextes de soins ou à des périodes futures. La validation externe permet de déterminer si un modèle entraîné sur des données de centres hospitaliers universitaires conserve sa précision dans les hôpitaux de proximité, ou si les variations géographiques dans la présentation de la maladie affectent ses performances.
Les modèles de prédiction du risque cardiovasculaire publiés présentent une forte capacité de discrimination ; les modèles validés atteignent des valeurs d’indice c comprises entre 0,84 et 0,87, quelle que soit la stratégie de modélisation. La cohérence entre les approches renforce la confiance, mais la légère variation observée entre les sous-groupes souligne l’importance d’une validation exhaustive.
Le contexte est également important. Un modèle de prédiction du cancer du poumon validé auprès d'une population de patients suivis en chirurgie thoracique et présentant une forte prévalence de cancer peut ne pas être aussi performant en consultation externe générale, où la prévalence de la maladie est plus faible. La prévalence de la maladie influence les valeurs prédictives positives et négatives, même lorsque la sensibilité et la spécificité restent constantes.
| Métrique de validation | Seuil cible | Signification clinique |
|---|---|---|
| Facteur de rétrécissement global | ≥0,9 | Optimisme minimal quant aux effets prédictifs |
| Différence R² (continue) | ≤0,05 | Variance expliquée stable |
| Différence R² (binaire) | ≤0,05 | Performances de classification constantes |
| Score Brier (binaire) | 0–0,25 | 0 = parfait, 0,25 = non informatif |
| Marge SD résiduelle | ≤10% | Estimation précise de la variabilité |
Défis de mise en œuvre qui comptent vraiment
La théorie, c'est une chose. La mise en œuvre, c'en est une autre.
Obstacles liés à la qualité et à l'intégration des données
La qualité des modèles prédictifs dépend de celle de leurs données d'entraînement. Les bases de données d'essais cliniques souffrent souvent de valeurs manquantes, d'un codage incohérent, de biais de sélection et d'une diversité limitée. Les données des dossiers médicaux électroniques présentent leurs propres problèmes : variabilité de la documentation, inexactitudes des codes de facturation et différences structurelles entre les systèmes de dossiers médicaux électroniques.
L'intégration de données provenant de sources multiples exige un nettoyage, une normalisation et une validation approfondis. C'est un travail ingrat, mais déterminant pour la validité des prédictions : seront-elles généralisables ou échoueront-elles lamentablement face à la complexité du monde réel ?.
Compromis entre interprétabilité et performance des modèles
Les architectures d'apprentissage automatique complexes surpassent souvent les modèles statistiques plus simples en termes de précision prédictive. Cependant, cet avantage se fait au détriment de l'interprétabilité. Les organismes de réglementation et les comités d'éthique de la recherche souhaitent comprendre pourquoi un modèle produit certaines prédictions, notamment lorsque celles-ci ont une incidence sur les décisions relatives à la sécurité des patients.
Les modèles linéaires et les arbres de décision offrent de la transparence. Les réseaux neuronaux profonds offrent de l'opacité. Le choix optimal dépend de l'application spécifique, des exigences réglementaires et des ressources de validation disponibles.
Considérations relatives à l'équité et aux préjugés
Les modèles prédictifs peuvent perpétuer ou amplifier les inégalités existantes en matière de santé si les données d'entraînement sous-représentent certaines populations ou si les variables prédictives sont corrélées à des caractéristiques protégées. Leur mise en œuvre doit intégrer les considérations d'équité dès leur conception et jusqu'à leur déploiement, en évaluant régulièrement la performance des modèles auprès de différents sous-groupes démographiques.
Les recommandations de la FDA abordent explicitement cette préoccupation, en recommandant aux promoteurs d'évaluer si les systèmes d'IA fonctionnent de manière cohérente au sein des sous-populations de patients et des contextes cliniques pertinents.
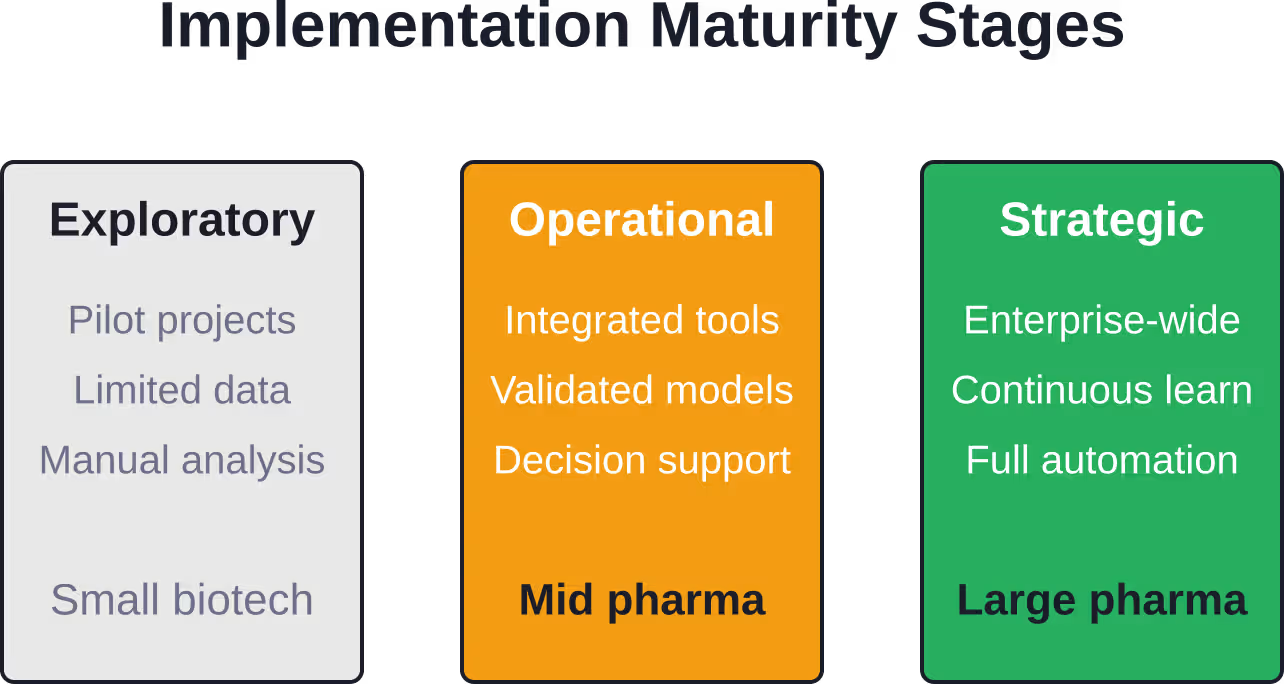
État actuel de l'adoption
Les entreprises pharmaceutiques et les organismes de recherche sous contrat ont dépassé le stade des projets pilotes. L'analyse prédictive influence désormais les décisions relatives aux essais cliniques, et les organisations mettent en place des équipes dédiées à la science des données et investissent dans les infrastructures analytiques.
Cela dit, l'adoption reste inégale. Les grandes entreprises pharmaceutiques, disposant de vastes bases de données d'essais cliniques et de solides compétences en analyse de données, sont à l'avant-garde. Les petites entreprises de biotechnologie et les centres de recherche universitaires sont confrontés à des obstacles plus importants en termes de ressources.
L'écosystème technologique continue d'évoluer rapidement. Les plateformes d'analyse basées sur le cloud, les approches d'apprentissage fédéré qui préservent la confidentialité des données et les modèles de base pré-entraînés adaptés aux applications cliniques gagnent tous en popularité.
Étapes pratiques pour démarrer
Les organisations qui découvrent l'analyse prédictive n'ont pas besoin de tout construire de zéro. Commencez par des cas d'usage bien définis et à fort impact, où la disponibilité des données est importante et la faisabilité de la validation est évidente.
- L'optimisation du recrutement des patients constitue un point d'entrée accessible. Les données historiques d'inscription, les indicateurs de performance des sites et les taux d'échec du dépistage fournissent de riches ensembles de données d'entraînement pour des modèles prédictifs relativement simples.
- L'évaluation de la faisabilité du protocole vient ensuite. L'analyse des protocoles antérieurs au regard des calendriers d'inscription réels révèle des tendances qui éclairent les décisions de conception futures. Cela ne nécessite pas d'algorithmes complexes : même des modèles de régression simples s'avèrent utiles lorsqu'ils sont appliqués systématiquement.
- Le développement des compétences internes est plus important que l'achat de logiciels. Il est essentiel de former les équipes opérationnelles cliniques à interpréter les résultats des modèles, à remettre en question les hypothèses et à intégrer les prédictions dans leurs processus décisionnels. Même le meilleur modèle prédictif est inutile si les parties prenantes ne lui font pas confiance ou ne savent pas comment exploiter ses enseignements.
- Les partenariats avec des centres hospitalo-universitaires, des organismes de recherche sous contrat dotés de capacités d'analyse ou des fournisseurs de technologies peuvent accélérer l'apprentissage. Il est cependant essentiel de préserver la maîtrise des compétences clés. L'analyse prédictive permettra de plus en plus aux entreprises de développement de médicaments performantes de se distinguer de celles qui rencontrent des difficultés.
Avoir hâte de
La tendance est claire. L'acceptation réglementaire des systèmes d'aide à la décision basés sur l'IA ne cesse de progresser. La disponibilité des données augmente constamment. Les capacités de calcul s'améliorent sans cesse. Les organisations qui développent dès maintenant des capacités d'analyse prédictive robustes bénéficieront d'avantages considérables par rapport à leurs concurrents qui s'appuient encore sur l'intuition et les tableurs.
Mais attendez.
La technologie seule ne résoudra pas les problèmes d'efficacité des essais cliniques. Les modèles prédictifs nécessitent une mise en œuvre réfléchie, une validation continue et une intégration à l'expertise humaine. L'objectif n'est pas de remplacer le jugement clinique, mais de le compléter par des données quantitatives auparavant inaccessibles.
Comme l'a souligné la FDA dans ses recommandations, l'IA et l'apprentissage automatique transforment le paysage des essais cliniques. Cette transformation offre des opportunités aux organisations prêtes à investir dans l'infrastructure, les talents et les changements culturels nécessaires pour que la prise de décision fondée sur les données devienne une pratique courante et non plus exceptionnelle.
La question n'est pas de savoir si l'analyse prédictive va transformer les essais cliniques, mais plutôt si certaines organisations prendront l'initiative de cette transformation ou s'efforceront de rattraper leur retard plus tard, lorsque la pression concurrentielle ne leur laissera pas d'autre choix.
Questions fréquemment posées
Quels types de données les modèles d'analyse prédictive utilisent-ils dans les essais cliniques ?
Les modèles intègrent généralement des bases de données historiques d'essais cliniques, des dossiers médicaux électroniques, des données de remboursement de soins, des registres de maladies, des informations génomiques et des données probantes issues de la pratique clinique. Les sources de données spécifiques dépendent de la tâche de prédiction : les modèles de recrutement privilégient les caractéristiques démographiques des patients et les performances des centres d'essais, tandis que les modèles de sécurité privilégient les bases de données d'événements indésirables et les résultats de laboratoire.
Dans quelle mesure les modèles prédictifs des résultats des essais cliniques sont-ils précis ?
La précision varie considérablement selon l'application et la qualité du modèle. Les modèles de risque cardiovasculaire bien validés atteignent des valeurs d'indice c comprises entre 0,84 et 0,87, ce qui indique une forte capacité de discrimination entre les patients à haut risque et ceux à faible risque. En revanche, les modèles peu performants peuvent ne pas donner de meilleurs résultats que le hasard. Une validation externe sur des jeux de données indépendants est donc indispensable avant de se fier aux prédictions d'un modèle.
La FDA exige-t-elle des normes de validation spécifiques pour l'IA dans les essais cliniques ?
Les recommandations de la FDA de 2024 relatives à l'intelligence artificielle dans le développement des médicaments préconisent que les promoteurs démontrent que les modèles sont adaptés à l'objectif visé, correctement validés et documentés de manière transparente. Bien qu'aucun seuil numérique précis ne soit imposé, les cadres de validation publiés suggèrent des indicateurs tels que des facteurs de rétrécissement ≥ 0,9 et des différences de R² ≤ 0,05 pour les variables continues.
L'analyse prédictive peut-elle réduire les coûts des essais cliniques ?
Les rapports sectoriels font état d'économies potentielles substantielles grâce à une sélection optimisée des sites, une réduction des taux d'échec de sélection, une meilleure stratification des patients et une identification plus précoce des essais inutiles. Toutefois, la concrétisation de ces avantages exige un investissement initial dans l'infrastructure de données, le développement et la validation des modèles ; or, toutes les applications ne sont pas rentables.
Quelle est la différence entre l'analyse prédictive et l'apprentissage automatique dans les procès ?
L'analyse prédictive est la discipline plus large qui consiste à utiliser les données pour prévoir les résultats futurs. L'apprentissage automatique représente des approches algorithmiques spécifiques au sein de l'analyse prédictive, qui permettent d'apprendre automatiquement des modèles à partir des données. Tout apprentissage automatique relève de l'analyse prédictive, mais toutes les analyses prédictives n'utilisent pas l'apprentissage automatique ; la régression statistique traditionnelle en fait également partie.
Comment les organisations gèrent-elles les biais dans les modèles prédictifs ?
Les bonnes pratiques consistent notamment à évaluer la performance du modèle au sein de sous-groupes démographiques, à s'assurer que les données d'entraînement représentent des populations diversifiées, à vérifier la corrélation des variables prédictives avec les caractéristiques protégées et à mettre en place des processus de gouvernance intégrant les considérations d'équité dès la conception du modèle et jusqu'à son déploiement. Les recommandations de la FDA préconisent explicitement d'évaluer la performance auprès des sous-populations de patients concernées.
Quelles compétences les équipes doivent-elles posséder pour mettre en œuvre l'analyse prédictive ?
La réussite de la mise en œuvre requiert des data scientists experts en statistiques et en apprentissage automatique, des spécialistes du domaine clinique maîtrisant le déroulement des essais cliniques et le contexte médical, des ingénieurs de données capables d'intégrer et de nettoyer des sources de données hétérogènes, ainsi que des spécialistes de la gestion du changement aptes à favoriser l'adhésion des parties prenantes sceptiques. Aucune personne n'a besoin de posséder à elle seule toutes ces compétences ; l'équipe doit les réunir.
Conclusion
L'analyse prédictive est passée du stade de la curiosité expérimentale à celui de nécessité opérationnelle dans les essais cliniques. Les recommandations officielles de la FDA, les cadres de validation publiés et le nombre croissant d'applications concrètes témoignent d'un changement fondamental dans la conception et la réalisation des essais.
Les organisations qui mettent en place une infrastructure de données, développent une expertise en validation et intègrent des analyses prédictives dans leurs processus décisionnels constatent déjà des améliorations tangibles en matière d'efficacité du recrutement, de faisabilité des protocoles et de résultats pour les patients. Celles qui tardent à agir s'exposent à un désavantage concurrentiel croissant, leurs concurrents bénéficiant de manière exponentielle des approches fondées sur les données.
Cette technologie continuera de s'améliorer. La véritable question est de savoir si les organisations développeront les compétences nécessaires pour l'exploiter efficacement. Il est essentiel de commencer par des cas d'usage bien définis, d'investir dans une validation rigoureuse et de privilégier l'intégration aux flux de travail existants plutôt que le remplacement complet des processus actuels.
L'avenir des essais cliniques est prévisible de manière quantitative. Les organisations qui intègrent systématiquement cette réalité seront à la pointe du développement des médicaments de demain.
